
新药研发是一个漫长而昂贵的过程,从开展最初的临床测试到新产品通过审批上市平均要花费8年的时间。各国药监部门对新药上市有严格的审批标准,新药上市前新药开发人员必须提供充足的药物安全性和有效性数据。新药上市申请失败,对防止无效或有害新药进入市场、维护患者生命安全具有重要意义。但是,许多新药上市失败,并不是因为药物不安全或无效,而是由于厂商提供给FDA的新药信息不足以支持新药上市。由于新药上市申请失败或延迟上市将会增加研发成本,因此对于企业而言,在递交新药上市申请时预先掌握新药信息不足主要体现在哪些方面,对于提高新药上市申请的成功率具有重要意义。
美国FDA的 Leonard V. Sacks等研究人员系统梳理了2000年10月1日至2012年9月30日之间向美国FDA药物评审中心提交的所有新分子实体上市申请。对失败的新药上市申请,研究人员详细研读了FDA的信函、文件等可以获得的资料,对新药上市申请失败的原因进行了深入的分析。
一、2000-2012年美国FDA新分子实体药物上市申请审批概况
2000年10月1日至2012年9月30日这12年中,共有332个新分子实体药物向美国FDA药物评审中心提交了新药上市申请。剔除23个非治疗药物(如诊断试剂)和7个在FDA决策前药厂自动撤销申请的新药外,余下的302个新分子实体药物中,151个(50%)新药通过第一轮审批顺利上市。
图1 2000-2012年美国FDA新分子实体药物上市申请结果分析
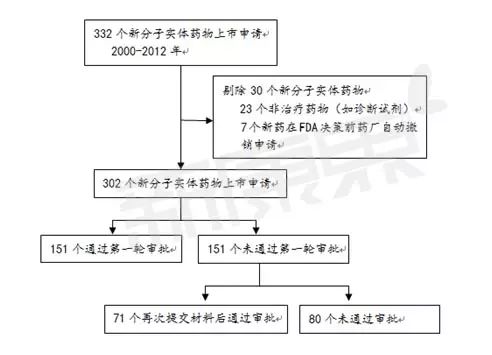
截止到2013年6月30日,第一轮申请失败的151个新分子实体药物中,87个新药(57.6%)针对同一个适应症再次提交了新药上市申请。55个新药(63.2%)在第二轮申请中获得批准,13个新药(14.9%)在第三轮申请中获得批准, 3个新药(3.4%)通过后来的多次申请终于获得批准。 在第一轮申请失败后,71个(47.0%)通过再次提交材料最终获得上市的新药平均多耗费435天(47 - 2374天)。
二、导致新药上市申请失败的主要原因
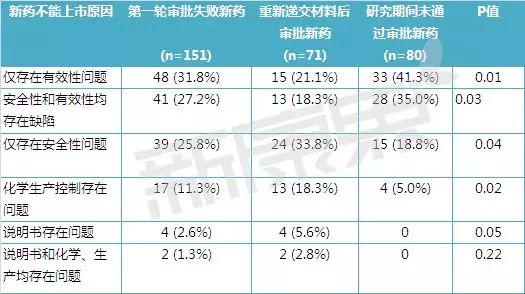
表1中详细分析了第一轮申请失败的151个新分子实体药物在安全性、有效性、说明书、化学生产控制中存在的问题。89个新药存在有效性问题,其中48个新药仅存在有效性问题,41个新药同时存在有效性和安全性问题;80个新药存在安全性问题,其中39个新药仅存在安全性问题,41个新药同时存在有效性和安全性问题;19个新药存在化学生产控制问题;6个新药存在说明书问题。从未批准新药和延迟批准新药的安全性问题发生率接近,80个从未批准新药中43个药物(53.8%)存在安全性问题,71个延迟批准新药中37 个药物(52.1%)存在安全性问题。 然而,从未批准新药有效性缺陷的发生率要显着高于延迟批准新药。80个从未批准新药中有61个药物(76.3%)存在有效性问题,71个延迟批准新药中28 个药物(39.4%)存在有效性问题。48个只存在有效性问题的新药中31.3%的新药通过后期审批上市,而39个只存在安全性问题的新药中61.5%的新药通过后期审批上市。
表1 新药上市申请第一轮失败的原因统计
(一)剂量问题导致新药上市申请失败
第一轮申请失败的新药中,24个(15.9%)新药因为没有最佳服用剂量而失败。这些药物绝大多为慢性疾病治疗药物,如癫痫新药(3个),止痛和消炎新药(2个),哮喘新药(2个)、高血压新药(1个)、心绞痛新药(1个),因此FDA驳回了新药上市申请,让公司继续探索其他最佳的药物剂量。
表2 新药上市申请主要存在的有效性缺陷统计
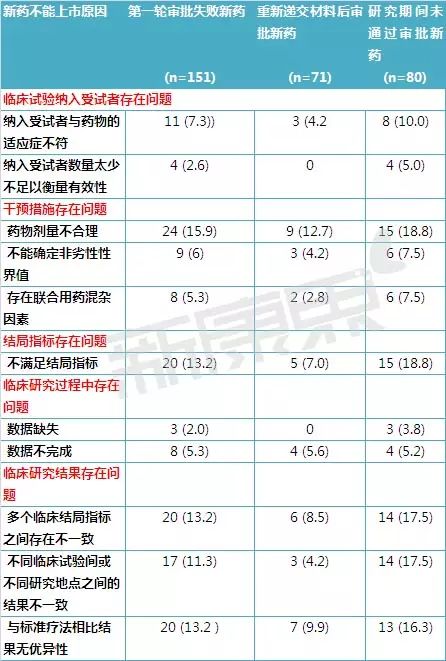
(二)有效性问题导致新药上市申请失败
11个(7.3%)新药的上市申请失败是因为纳入的受试者与药物的适应症不符。
20个(13.2%)新药上市申请失败是因为临床结局指标不令人满意。有些药物的临床结局指标不能很好的评估药物治疗效果、有些药物的临床结局指标采集的时间点存在问题。例如临床结局指标采集的时间太早不足以反映药物在整个治疗周期的疗效;FDA评审专家和科研人员对治疗成功的定义不同;癌症新药的临床结局指标设定为无进展生存期而不是整体生存期;有些新药的临床结局指标设定为病理指标的改变(如用力肺活量、尿酸),但是病理指标改变与临床疗效之间并没有直接关联。
20个(13.2%)新药的上市申请失败是因为多个临床结局指标之间存在不一致。17个(11.3%)新药上市申请失败是因为在不同地区不同人群中的临床试验结果存在不一致。在这种情况下,新药仅对部分地区的部分人群有效,而对其他亚种人群无效果。
20个(13.2%)新药尽管与安慰剂对比存在治疗优越性,但是与标准疗法对比则功效不足。如心律失常、癌症和精神分裂症已经上市了疗效更好的药物,因此这类新药上市时除非有更好的疗效或更安全性,否则很难能上市。
(三)安全性问题导致新药上市申请失败
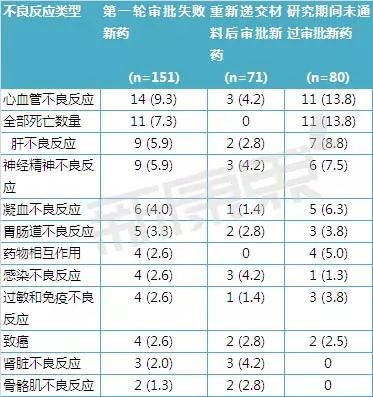
心血管系统不良反应是导致新药上市申请失败最常见的安全性问题。其他不良反应包括肝不良反应、神经精神不良反应、凝血不良反应、胃肠道不良反应等,具体见表3。
表3 新药上市申请主要存在的安全性缺陷统计
(四)说明书和化学、生产问题导致新药上市申请失败
23个新药尽管有效性和安全性都没有问题,但是由于说明书、化学生产和控制方面存在问题,因而没能在第一轮审批中顺利上市。化学生产和控制问题包括药物不溶解、药物不稳定、内毒素高、生产设施存在问题等。 |
